Prazeodymjest trzecim najliczniej występującym pierwiastkiem lantanowca w układzie okresowym pierwiastków chemicznych, którego zawartość w skorupie ziemskiej wynosi 9,5 ppm, czyli mniej niżcer, itr,lantan, Iskand. Jest to piąty najliczniej występujący pierwiastek w pierwiastkach ziem rzadkich. Ale tak jak jego imię,prazeodymjest prostym i pozbawionym ozdób przedstawicielem rodziny metali ziem rzadkich.
CF Auer Von Welsbach odkrył prazeodym w 1885 roku.
W 1751 roku szwedzki mineralog Axel Fredrik Cronstedt odkrył ciężki minerał w rejonie górniczym Bastnäs, który później nazwano cerytem. Trzydzieści lat później piętnastoletni Vilhelm Hisinger z rodziny, która była właścicielem kopalni, wysłał swoje próbki do Carla Scheele, ale nie odkrył żadnych nowych pierwiastków. W 1803 roku, po tym jak Singer został kowalem, powrócił na teren górniczy z Jönsem Jacobem Berzeliusem i oddzielił nowy tlenek, planetę karłowatą Ceres, którą odkryli dwa lata temu. Cer został niezależnie oddzielony przez Martina Heinricha Klaprotha w Niemczech.
W latach 1839–1843 szwedzki chirurg i chemik Carl Gustaf Mosander odkrył, żetlenek cerubyła mieszaniną tlenków. Oddzielił dwa inne tlenki, które nazwał lanthana i didymia „didymia” (co po grecku oznacza „bliźniaki”). Częściowo rozłożyłazotan cerupróbkę poprzez prażenie jej na powietrzu, a następnie poddanie jej działaniu rozcieńczonego kwasu azotowego w celu uzyskania tlenku. Metale, które tworzą te tlenki, są zatem nazywanelantanIprazeodym.
W 1885 roku CF Auer Von Welsbach, Austriak, który wynalazł osłonę gazową lampy torowo-cerowej, pomyślnie oddzielił „prazeodym neodymowy”, „bliźniaki syjamskie”, z których zielona sól prazeodymu i różowa sól neodymu zostały oddzielone i uznane za dwa nowe pierwiastki. Jeden z nich nosi nazwę „Praseodymium”, co pochodzi od greckiego słowa prason, oznaczającego zielony związek, ponieważ roztwór wody z solą prazeodymu będzie miał jasnozielony kolor; Drugi pierwiastek nosi nazwę „Neodymowy„. Udane rozdzielenie „bliźniaków syjamskich” pozwoliło im na niezależne zaprezentowanie swoich talentów.
Srebrnobiały metal, miękki i ciągliwy. Prazeodym ma heksagonalną strukturę krystaliczną w temperaturze pokojowej. Odporność na korozję w powietrzu jest większa niż w przypadku lantanu, ceru, neodymu i europu, ale po wystawieniu na działanie powietrza powstaje warstwa kruchego czarnego tlenku, a próbka metalu prazeodymu o wielkości jednego centymetra ulega całkowitej korozji w ciągu około roku.
Jak większośćpierwiastki ziem rzadkich, prazeodym najprawdopodobniej tworzy stopień utlenienia +3, który jest jego jedynym stabilnym stanem w roztworach wodnych. Prazeodym występuje w stopniu utlenienia +4 w niektórych znanych związkach stałych, a w warunkach rozdzielenia matrycy może osiągnąć unikalny stopień utlenienia +5 wśród pierwiastków lantanowców.
Wodny jon prazeodymu ma barwę limonkowozieloną, a wiele zastosowań przemysłowych prazeodymu wiąże się z jego zdolnością do filtrowania żółtego światła w źródłach światła.
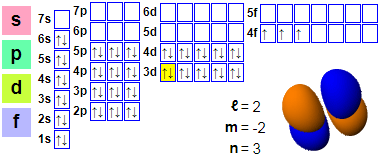
Układ elektroniczny prazeodymu
Emisje elektroniczne:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f3
59 elektronów prazeodymu jest ułożonych jako [Xe] 4f36s2. Teoretycznie wszystkie pięć zewnętrznych elektronów może być użytych jako elektrony walencyjne, ale użycie wszystkich pięciu zewnętrznych elektronów wymaga ekstremalnych warunków. Generalnie prazeodym emituje tylko trzy lub cztery elektrony w swoich związkach. Prazeodym jest pierwszym pierwiastkiem lantanowca o konfiguracji elektronicznej zgodnej z zasadą Aufbau. Jego orbital 4f ma niższe poziomy energii niż orbital 5d, co nie ma zastosowania do lantanu i ceru, ponieważ nagłe skurczenie orbitalu 4f nie występuje aż do lantanu i nie jest wystarczające, aby uniknąć zajęcia powłoki 5d w cerze. Jednakże stały prazeodym wykazuje konfigurację [Xe] 4f25d16s2, w której jeden elektron na powłoce 5d przypomina wszystkie inne trójwartościowe pierwiastki lantanowców (z wyjątkiem europu i iterbu, które są dwuwartościowe w stanach metalicznych).
Podobnie jak większość pierwiastków lantanowców, prazeodym zwykle wykorzystuje tylko trzy elektrony jako elektrony walencyjne, a pozostałe elektrony 4f mają silny efekt wiążący: dzieje się tak, ponieważ orbita 4f przechodzi przez obojętny rdzeń ksenonowy elektronu, aby dotrzeć do jądra, a następnie przez 5d i 6s, i wzrasta wraz ze wzrostem ładunku jonowego. Jednak prazeodym może nadal tracić czwarty, a nawet sporadycznie piąty elektron walencyjny, ponieważ pojawia się bardzo wcześnie w układzie lantanowców, gdzie ładunek jądrowy jest nadal wystarczająco niski, a energia podpowłoki 4f jest wystarczająco wysoka, aby umożliwić usunięcie większej ilości elektronów walencyjnych.
Prazeodym i wszystkie pierwiastki lantanowców (z wyjątkiemlantan, iterbIlutet, nie ma niesparowanych elektronów 4f) są paramagnetyzmem w temperaturze pokojowej. W przeciwieństwie do innych metali ziem rzadkich, które wykazują antyferromagnetyczne lub ferromagnetyczne uporządkowanie w niskich temperaturach, prazeodym jest paramagnetyzmem we wszystkich temperaturach powyżej 1K
Zastosowanie Prazeodymu
Prazeodym jest najczęściej wykorzystywany w formie mieszanej ziem rzadkich, jako środek oczyszczający i modyfikujący materiały metalowe, katalizatory chemiczne, metale ziem rzadkich w rolnictwie itd.Prazeodym neodymowyjest najbardziej podobną i trudną do rozdzielenia parą pierwiastków ziem rzadkich, którą trudno rozdzielić metodami chemicznymi. Produkcja przemysłowa zwykle wykorzystuje metody ekstrakcji i wymiany jonowej. Jeśli są one używane parami w postaci wzbogaconego prazeodymu neodymu, ich wspólność może być w pełni wykorzystana, a cena jest również niższa niż w przypadku produktów jednoelementowych.
Stop prazeodymu i neodymu(metal prazeodymowy (neodym metal)stał się niezależnym produktem, który może być stosowany zarówno jako materiał na magnesy trwałe, jak i dodatek modyfikujący do stopów metali nieżelaznych. Aktywność, selektywność i stabilność katalizatora krakingu ropy naftowej można poprawić, dodając koncentrat prazeodymu neodymu do sita molekularnego zeolitu Y. Jako dodatek modyfikujący tworzywa sztuczne, dodanie wzbogacenia prazeodymu neodymu do politetrafluoroetylenu (PTFE) może znacznie poprawić odporność PTFE na zużycie.
Rzadka ziemiamateriały z magnesami trwałymi są obecnie najpopularniejszym obszarem zastosowań metali ziem rzadkich. Sam prazeodym nie jest wybitnym materiałem z magnesami trwałymi, ale jest doskonałym pierwiastkiem synergistycznym, który może poprawić właściwości magnetyczne. Dodanie odpowiedniej ilości prazeodymu może skutecznie poprawić wydajność materiałów z magnesami trwałymi. Może również poprawić wydajność antyoksydacyjną (odporność na korozję w powietrzu) i właściwości mechaniczne magnesów i jest szeroko stosowany w różnych urządzeniach elektronicznych i silnikach.
Prazeodym może być również stosowany do szlifowania i polerowania materiałów. Jak wszyscy wiemy, czysty proszek polerski na bazie ceru jest zwykle jasnożółty, co jest wysokiej jakości materiałem polerskim do szkła optycznego i zastąpił czerwony proszek tlenku żelaza, który ma niską wydajność polerowania i zanieczyszcza środowisko produkcyjne. Ludzie odkryli, że prazeodym ma dobre właściwości polerujące. Proszek polerski ziem rzadkich zawierający prazeodym będzie miał czerwonobrązowy kolor, znany również jako „czerwony proszek”, ale ten czerwony kolor nie jest czerwonym tlenkiem żelaza, ale ze względu na obecność tlenku prazeodymu kolor proszku polerskiego ziem rzadkich staje się ciemniejszy. Prazeodym był również stosowany jako nowy materiał szlifierski do produkcji ściernic korundowych zawierających prazeodym. W porównaniu z białym tlenkiem glinu wydajność i trwałość można poprawić o ponad 30% podczas szlifowania stali konstrukcyjnej węglowej, stali nierdzewnej i stopów wysokotemperaturowych. Aby obniżyć koszty, w przeszłości jako surowce często stosowano materiały wzbogacone prazeodymem i neodymem, stąd nazwa „koło ścierne prazeodymowo-neodymowo-korundowe”.
Kryształy krzemianowe domieszkowane jonami prazeodymu zostały wykorzystane do spowolnienia impulsów świetlnych do kilkuset metrów na sekundę.
Dodanie tlenku prazeodymu do krzemianu cyrkonu spowoduje, że stanie się on jasnożółty i może być stosowany jako pigment ceramiczny – żółcień prazeodymowa. Żółć prazeodymowa (Zr02-Pr6Oll-Si02) jest uważana za najlepszy żółty pigment ceramiczny, który pozostaje stabilny w temperaturze do 1000 ℃ i może być stosowany w procesach jednorazowych lub ponownego wypalania.
Prazeodym jest również stosowany jako barwnik do szkła, o bogatych kolorach i dużym potencjale rynkowym. Można produkować zielone produkty szklane z prazeodymu o jasnych kolorach zielonego pora i szczypiorku, które można wykorzystać do produkcji zielonych filtrów, a także do szkła artystycznego i rzemieślniczego. Dodanie tlenku prazeodymu i tlenku ceru do szkła może być stosowane jako gogle do spawania. Siarczek prazeodymu może być również stosowany jako zielony barwnik do plastiku.
Czas publikacji: 29-05-2023